Mudanças entre as edições de "QMC1-EngTel (Plano de Ensino)"
Ir para navegação
Ir para pesquisar
| Linha 1: | Linha 1: | ||
{{Cab1-IF-SC-Engtelecom}} | {{Cab1-IF-SC-Engtelecom}} | ||
<BIG><center> | <BIG><center> | ||
| − | '''Plano de Ensino de | + | '''Plano de Ensino de 2012-2''' |
</center></BIG> | </center></BIG> | ||
| Linha 13: | Linha 13: | ||
;Objetivos | ;Objetivos | ||
| − | : | + | :... |
| − | |||
| − | |||
| − | |||
| − | |||
;Ementa | ;Ementa | ||
| Linha 26: | Linha 22: | ||
;Cronograma de atividades | ;Cronograma de atividades | ||
| − | + | <!--Colar conteúdo da aba PE-Wiki do Diário Eletrônico --> | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
;Estratégias de ensino utilizadas | ;Estratégias de ensino utilizadas | ||
| − | : | + | :... |
;Critérios e instrumentos de avaliação | ;Critérios e instrumentos de avaliação | ||
| − | : | + | :... |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
;Atividades Complementares | ;Atividades Complementares | ||
| Linha 85: | Linha 37: | ||
;Bibliografia Complementar | ;Bibliografia Complementar | ||
| − | |||
| − | |||
;Professores Responsáveis | ;Professores Responsáveis | ||
| − | :Prof. [[ | + | :Prof. [[Giovani Pakuszewski]] |
{{ENGTELECO}} | {{ENGTELECO}} | ||
Edição das 18h16min de 28 de junho de 2013

|
MINISTÉRIO DA EDUCAÇÃO |
Plano de Ensino de 2012-2
- Dados gerais
[[Arquivo:
|right | thumb |
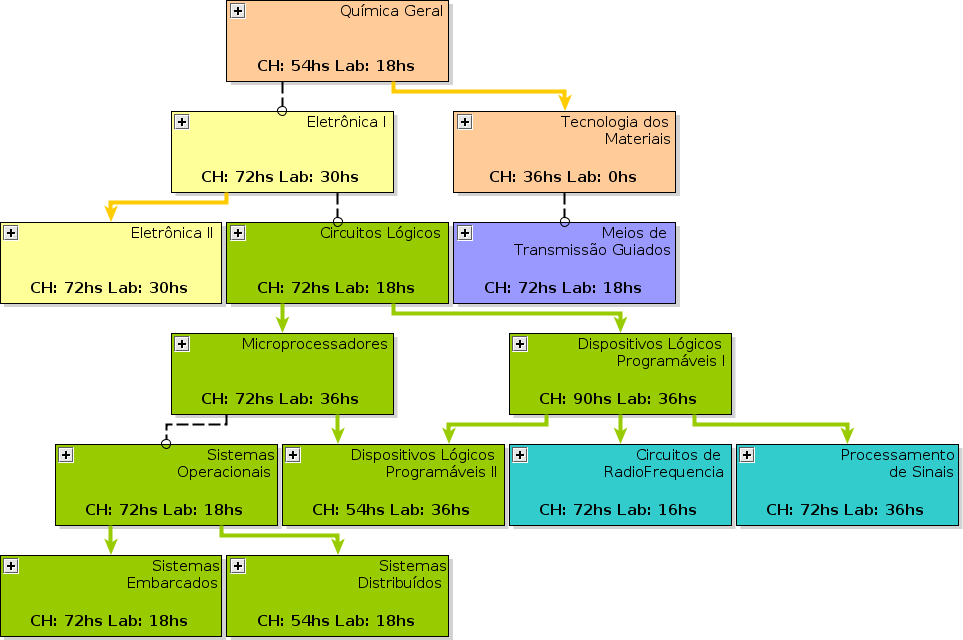
250px | UCs vizinhas]]
- COMPONENTE CURRICULAR: QMC1 - QUÍMICA GERAL
- CARGA HORÁRIA: 3 HORAS/SEMANA 54 HORAS. TEÓRICA = 36 HORAS. LABORATÓRIO = 18 HORAS
- PRÉ REQUISITOS:
- DISCIPLINAS SUCESSORAS: QMC2, ELA1*
- MÓDULO BÁSICO
- Objetivos
- ...
- Ementa
- Conceitos fundamentais da química. Estrutura da matéria. Periodicidade química: propriedades atômicas e tendências periódicas. Ligações químicas: ligação iônica, covalente, ligação metálica, forças inter e intramoleculares. Reações químicas. Introdução à química dos polímeros. Introdução à química do meio ambiente.
- Conteúdo Programático
- 1.Átomos, moléculas e íons (6h).
2.Estrutura eletrônica dos átomos (6h).
3. Conceitos básicos de ligações química (6h).
4. Forças intermoleculares, líquidos e sólidos (6h).
5. Materiais modernos (6h).
6. Reações em soluções aquosas (6h).
7. Química Ambiental: Atmosfera, quimica da troposfera (6h).
8. Avaliações (6h).
- Cronograma de atividades
- Estratégias de ensino utilizadas
- ...
- Critérios e instrumentos de avaliação
- ...
- Atividades Complementares
- Prever laboratórios (18h)
- Bibliografia Básica
- 1.BROWN, Theodore L. et al. Química: a ciência central. 9.ed. São Paulo: Pearson Prentice Hall, 2010. 972 p. ISBN 978-8587915420.
- Bibliografia Complementar
- Professores Responsáveis
- Prof. Giovani Pakuszewski